- 770.50 KB
- 2021-05-10 发布
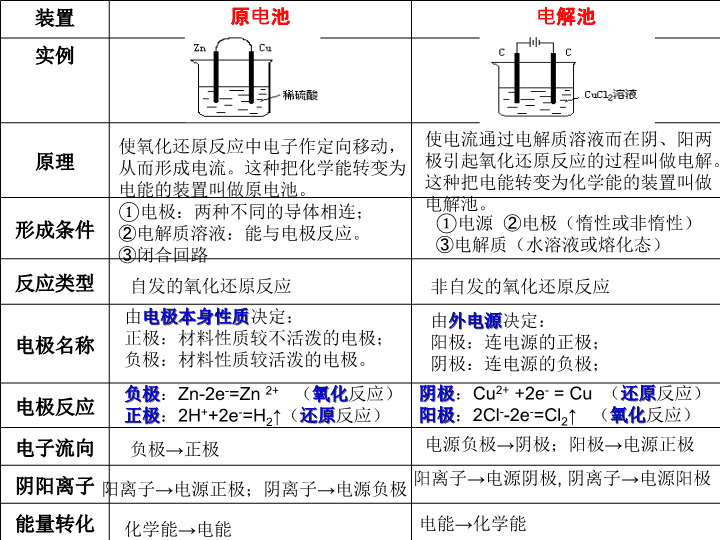
专题:电化学原理
装置
原电池
电解池
实例
原理
形成条件
反应类型
电极名称
电极反应
电子流向
阴阳离子
能量转化
使氧化还原反应中电子作定向移动,从而形成电流。这种把化学能转变为电能的装置叫做原电池。
①
电极:两种不同的导体相连;
②电解质溶液:能与电极反应。
③闭合回路
自发的氧化还原反应
由
电极本身性质
决定:
正极:材料性质较不活泼的电极;
负极:材料性质较活泼的电极。
负极
:
Zn-2e
-
=Zn
2+
(
氧化
反应)
正极
:
2H
+
+2e
-
=H
2
↑
(
还原
反应)
负极→正极
阳离子→电源正极;阴离子→电源负极
化学能→电能
使电流通过电解质溶液而在阴、阳两极引起氧化还原反应的过程叫做电解。这种把电能转变为化学能的装置叫做电解池。
①
电源 ②电极(惰性或非惰性)
③电解质(水溶液或熔化态)
非自发的氧化还原反应
由
外电源
决定:
阳极:连电源的正极;
阴极:连电源的负极;
阴极
:
Cu
2+
+2e
-
= Cu
(
还原
反应)
阳极
:
2Cl
-
-2e
-
=Cl
2
↑
(
氧化
反应)
电源负极→阴极;阳极→电源正极
阳离子→电源阴极
,
阴离子→电源阳极
电能→化学能
例
1
、
依据氧化还原反应:
2Ag
+
(aq)
+
Cu(s)
=
Cu
2
+
(aq)
+
2Ag(s)
设计的原电池如图所示:
⑴
电极
X
的材料是
;
电解质溶液
Y
是
;
⑵银电极为电池的
极,发生的电极反应为
;
X
电极上发生的电极
反应为
;
⑶外电路中的电子
是从
电极
流向
电极。
Cu
AgNO
3
正
Ag
+
+ e
-
= Ag
Cu - 2e
-
= Cu
2+
Cu
Ag
例
1
、
依据氧化还原反应:
2Ag
+
(aq)
+
Cu(s)
=
Cu
2
+
(aq)
+
2Ag(s)
设计的原电池如图所示:
⑴
电极
X
的材料是
;
电解质溶液
Y
是
;
⑵银电极为电池的
极,
发生的电极反应为
;
X
电极上发生的电极
反应为
;
⑶外电路中的电子
是从
电极
流向
电极。
Cu
AgNO
3
正
Ag
+
+ e
-
= Ag
Cu - 2e
-
= Cu
2+
Cu
Ag
题目解析:
考点:原电池装置判断
分值:
1+1+1
得分:
例
1
、
依据氧化还原反应:
2Ag
+
(aq)
+
Cu(s)
=
Cu
2
+
(aq)
+
2Ag(s)
设计的原电池如图所示:
⑴
电极
X
的材料是
;
电解质溶液
Y
是
;
⑵银电极为电池的
极,
发生的电极反应为
;
X
电极上发生的电极
反应为
;
⑶外电路中的电子
是从
电极
流向
电极。
Cu
AgNO
3
正
Ag
+
+ e
-
= Ag
Cu - 2e
-
= Cu
2+
Cu
Ag
题目解析:
考点:原电池电极反应方程式的书写
分值:
2+2
得分:
例
1
、
依据氧化还原反应:
2Ag
+
(aq)
+
Cu(s)
=
Cu
2
+
(aq)
+
2Ag(s)
设计的原电池如图所示:
⑴
电极
X
的材料是
;
电解质溶液
Y
是
;
⑵银电极为电池的
极,发生的电极反应为
;
X
电极上发生的电极
反应为
;
⑶
外电路中的电子
是从
电极
流向
电极
。
Cu
AgNO
3
正
Ag
+
+ e
-
= Ag
Cu - 2e
-
= Cu
2+
Cu
Ag
题目解析:
考点:原电池原理判断
分值:
1+1
得分:
考 纲 要 求
考点
分值
得分
电化学原理
(1)
原电池装置原理判断,原电池电极反应和电池反应方程式的书写
(2)
常见化学电源的种类,碱性锌锰干电池、铅蓄电池、燃料电池的工作原理及其应用价值
(3)
电解池装置原理判断,电解池电极判断与电极反应和电池反应方程式的书写
(4)
一些电解过程(如电解熔融氯化钠、饱和食盐水)实例工作原理分析及电极反应式书写与判断
(5)
了解电解原理在氯碱生产、金属精炼和电镀中的应用
例
2
、
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液
a
;
X
、
Y
是两块电极板,通过导线与直流电源相连。请回答以下问题:
a
A
X
Y
+
―
(
1
)若
X
、
Y
都是惰性电极,
a
是饱和
NaCl
溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中
①
X
的电极名称是
,电极反应式为
,在
X
极附近观察到的实验现象是
。
②
Y
的电极名称是
,电极反应式为
,检验该电极产物的方法是
。
③ 若
Y
电极改为铜棒,则
Y
电极反应式为
。
(
2
)如要用电解方法精炼粗铜,电解液
a
选用
CuSO
4
溶液,则
①
X
电极的材料是
,
电极反应式为
。
②
Y
电极的材料是
,电极反应式为
。
(说明:杂质发生的电极反应不必写出)
题目解析:
考点:电解池装置原理判断
电解池电极判断与电极反应方程式的书写
电解池原理的应用
分值:
得分:
例
2
、
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液
a
;
X
、
Y
是两块电极板,通过导线与直流电源相连。请回答以下问题:
a
A
X
Y
+
―
(
1
)若
X
、
Y
都是惰性电极,
a
是饱和
NaCl
溶液,实验开始时,同 时在两边各滴入几滴酚酞试液,则电解池中
①
X
的电极名称是
,电极反应式为
,在
X
极附近观察到的实验现象是
。
②
Y
的电极名称是
,电极反应式为
,检验该电极产物的方法是
。
③ 若
Y
电极改为铜棒,则
Y
电极反应式为
。
(
2
)如要用电解方法精炼粗铜,电解液
a
选用
CuSO
4
溶液,则
①
X
电极的材料是
,
电极反应式为
。
②
Y
电极的材料是
,电极反应式为
。
(说明:杂质发生的电极反应不必写出)
2H
2
O+2e
-
=H
2
↑+2OH
-
或
2H
+
+2e
-
=H
2
↑
阴极
放出气体,溶液变红
阳极
2Cl
-
—2e
-
=Cl
2
↑
把湿润的碘化钾淀粉试纸放在
Y
电极附近,试纸变蓝色
Cu—2e
-
=Cu
2+
Cu
—
2e
-
=Cu
2+
粗铜
Cu
2+
+
2e
-
=Cu
纯铜
考 纲 要 求
考点
分值
得分
电化学原理
(1)
原电池装置原理判断,原电池电极反应和电池反应方程式的书写
(2)
常见化学电源的种类,碱性锌锰干电池、铅蓄电池、燃料电池的工作原理及其应用价值
(3)
电解池装置原理判断,电解池电极判断与电极反应和电池反应方程式的书写
(4)
一些电解过程(如电解熔融氯化钠、饱和食盐水)实例工作原理分析及电极反应式书写与判断
(5)
了解电解原理在氯碱生产、金属精炼和电镀中的应用
例
3
、
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入
CH
4
和
O
2
,电解质为
KOH
溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氧化钠辖液电解实验,如图所示
:
回答下列问题:
(1)
甲烷燃料电池正极、负极的电极反应分别为
、
。
(2)
闭合
K
开关后,
a
、
b
电极上均有气体产生.其中
b
电极上得到的是
,电解氯化钠溶液的总反应方程式为
;
(3)
若每个电池甲烷通入量为
1 L(
标准状况
)
,且反应完全,则理论上通过电解池的电量为
(法拉第常数
F=9.65×l0
4
C
· mol
-1
列式计算
)
,最多能产生的氯气体积为
L(
标准状况
)
。
题目解析:
考点:燃料电池的工作原理;
电解原理与电池反应方程式的书写;
电解原理的有关计算
分值:
得分
例
3
、
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入
CH
4
和
O
2
,电解质为
KOH
溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氧化钠辖液电解实验,如图所示
:
回答下列问题:
(1)
甲烷燃料电池正极、负极的电极反应分别为
、
。
(2)
闭合
K
开关后,
a
、
b
电极上均有气体产生.其中
b
电极上得到的是
,电解氯化钠溶液的总反应方程式为
;
(3)
若每个电池甲烷通入量为
1 L(
标况
)
,且反应完全,则理论上通过电解池的电量为
(法拉第常数
F=9.65×l0
4
C
· mol
-1,
列式计算
)
,最多能产生的氯气体积为
L(
标况
)
。
2O
2
+ 4H
2
O +8e
-
= 8OH
-
,
CH
4
+
10OH
-
-
8e
-
= CO
3
2
-
+
7H
2
O
2NaCl
+
2H
2
O=2NaOH
+
H
2
↑
+
Cl
2
↑
电解
H
2
( 1L/22.4L/mol) ×8×9.65×10
4
C·mol
-1
= 3.45×10
4
C 4L
考 纲 要 求
考点
分值
得分
电化学原理
(1)
原电池装置原理判断,原电池电极反应和电池反应方程式的书写
(2)
常见化学电源的种类,碱性锌锰干电池、铅蓄电池、燃料电池的工作原理及其应用价值
(3)
电解池装置原理判断,电解池电极判断与电极反应和电池反应方程式的书写
(4)
一些电解过程(如电解熔融氯化钠、饱和食盐水)实例工作原理分析及电极反应式书写与判断
(5)
了解电解原理在氯碱生产、金属精炼和电镀中的应用
1
、按如图所示装置进行实验,
并回答下列问题:
(1)
判断装置的名称:
A
池为
________
,
B
池为
________
.
(2)
锌极为
________
,电极反应式为
________________
;
铜极为
___________
,电极反应式为
________________
;石墨棒
C
1
为
________
,电极反应式为
____ ____
;
石墨棒
C
2
附近产生的实验现象为
____ ___
.
(3)
当
C
2
极析出
224 mL
气体
(
标准状况下
)
,锌的质量变化
(
增加或减少
)
了
________g
.
CuSO
4
溶液的质量变化
(
增加或减少
)
了
________g.
【
迁移应用
】
原电池
电解池
负极
Zn
-
2e
-
===
Zn
2
+
正极
Cu
2
+
+
2e
-
===
Cu
阳极
2Cl
-
-
2e
-
===
Cl
2
↑
有无色气体产生,附近溶液变为红色
0.65
0.01
【
迁移应用
】
2
、
Li-SOCl
2
电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是
LiAICl
4
—SOCl
2
。电池的总反应可表示为:
4Li+2SOCl
2
= 4LiCl +S +SO
2
。请回答下列问题:
(1)
电池的负极材料为
,发生的电极反应为
;
(2)
电池正极发生的电极反应
为
;
锂
【
迁移应用
】
3
、
Mg-AgCl
电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:
2AgCl + Mg
=
Mg
2
+
+ 2Ag + 2Cl
-
。有关该电池的说法正确的是
( )
A
.
Mg
为电池的正极
B
.负极反应为
AgCl + e
-
=
Ag + Cl
-
C
.不能被
KCl
溶液激活
D
.可用于海上应急照明供电
D
4
、
关于铅蓄电池的说法正确的是
( )
A
.在放电时,正极发生的反应是
Pb(s) + SO
4
2-
(
aq
)
= PbSO
4
(s) + 2e
-
B
.在放电时,该电池的负极材料是铅板
C
.在充电时,电池中硫酸的浓度不断变小
D
.在充电时,阳极发生的反应是
PbSO
4
(s)+2e
-
= Pb(s)+ SO
4
2-
(
aq
)
B
5
、
下图所示的电解池
I
和
II
中,
a
、
b
、
c
和
d
均为
Pt
电极。电解过程中,电极
b
和
d
上没有气体逸出,但质量均增大,且增重
b
>
d
。符合上述实验结果的盐溶液是
( )
选项
X
Y
A
.
MgSO
4
CuSO
4
B
.
AgNO
3
Pb(NO
3
)
2
C
.
FeSO
4
Al
2
(SO
4
)
3
D
.
CuSO
4
AgNO
3
X
盐
溶液
a
b
Y
盐
溶液
c
d
电解池
I
电解池
Ⅱ
D
【
迁移应用
】
6
、
利用电解法可将含有
Fe
、
Zn
、
Ag
、
Pt
等杂质的粗铜提纯,下列叙述正确的是
( )
A.
电解时以精铜作阳极
B
.电解时阴极发生还原反应
C
.粗铜连接电源负极,其电极反应是
Cu=Cu
2+
+2e-
D
.电解后,电解槽底部会形成含少量
Ag
、
Pt
等金属的阳极泥
BD
【
迁移应用
】
【
迁移应用
】
7
、
一种充电电池放电时的电极反应为
H
2
+2OH
-
-2e
-
=2H
2
O; NiO(OH)+H
2
O+e-=Ni(OH)
2
+OH
-
当为电池充电时,与外电源正极连接的电极上发生的反应是
( )
A. H
2
O
的还原
B. NiO(OH)
的还原
C. H
2
的氧化
D. Ni(OH)
2
的氧化
D
主干知识小结
练习:优化探究
P
31-32
谢谢指导
再见