- 279.00 KB
- 2021-04-28 发布
吉林省通化市梅河口市博文学校2019-2020学年高一上学期期末考试试题
可能用到的相对原子质量:H-1 O-16 N-14 C-12 Ca-40 S-32 Al-27 Mg-24 Fe-56 Na-23 Cl-35.5 Fe-56
第I卷 选择题
一.选择题
1.化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是( )
A. 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
B. 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂
C. 2010年11月广州亚运会燃放的焰火是某些金属元素焰色反应所呈现出来的色彩
D. 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁
【答案】A
【解析】
【详解】A、为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入硫酸亚铁,生石灰和硅胶不具有还原性,不能作抗氧化剂,放入生石灰或硅胶目的是作干燥剂,A错误;
B、小苏打受热易分解生成二氧化碳气体,是制作馒头和面包等糕点的膨松剂,小苏打可与盐酸反应,是治疗胃酸过多的一种药剂,B正确;
C、焰火是某些金属元素焰色反应所呈现出来的特殊颜色,C正确;
D、我国使用最早的合金材料是青铜,钢铁是目前世界上使用量最大的合金材料,D正确;
答案选A。
2. 用特殊的方法把固体物质加工到纳米级的超细粉末粒子,然后制得纳米材料。下列分散系中分散质的微粒直径和这种粒子具有相同数量级的是( )
A. 溶液 B. 悬浊液 C. 胶体 D. 乳浊液
【答案】C
【解析】
详解】溶液中微粒直径小于1nm,浊液中微粒直径大于100nm,而胶体中微粒直径介于1nm和100nm之间,所以选项C正确;
答案选C。
3.分类法是一种行之有效、简单易行的科学方法。某同学用下表所示形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系。下列各组中,有错误的组合是( )
选项
甲
乙、丙、丁
A
常见干燥剂
浓硫酸、五氧化二磷、碱石灰
B
常见合金
不锈钢、焊锡、生铁
C
常见营养物质
蛋白质、维生素、无机盐
D
常见碱
烧碱、纯碱、熟石灰
【答案】D
【解析】
【详解】A.常见的干燥剂包括浓硫酸、P2O5、碱石灰等,A项正确;
B.不锈钢、焊锡、生铁、铝合金等是常见的合金,B项正确;
C.蛋白质、维生素、无机盐属于常见的营养物质,C项正确;
D.纯碱属于盐,不属于碱,D项错误;
答案选D。
4.用NA表示阿伏加德罗常数,以下各说法中不正确的是( )
A. 1mol铝作为还原剂可提供的电子数为3NA
B. 17g NH3中所含电子个数为10 NA
C. 22.4LN2分子中所含原子数为2 NA
D. 1L2mol·L-1的Mg(NO3)2溶液中含NO3-个数为4 NA
【答案】C
【解析】
【详解】A.铝是活泼金属,在化学反应中失3个电子,所以1mol铝作为还原剂可提供的电子数为3NA,A项正确;
B.17g NH3的物质的量为1mol,氨气是10电子分子,1mol氨气中所含电子个数为10 NA,B项正确;
C.没有说明是否处于标准状况,无法通过气体体积计算物质的量,C项错误;
D.硝酸镁属于盐,1L2mol·L-1的Mg(NO3)2溶液中含NO3-个数为4 NA,D项正确;
答案选C。
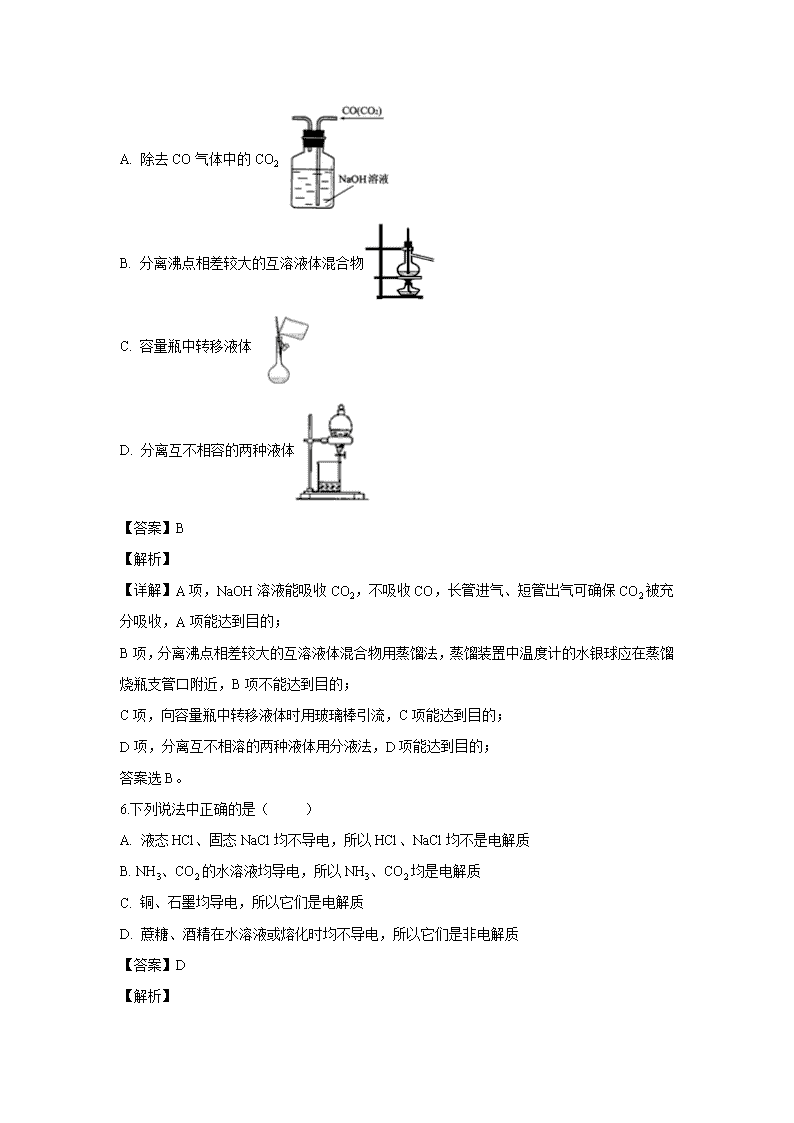
5.下列实验装置图所示的实验操作,不能达到相应的实验目的的是( )
A. 除去CO气体中的CO2
B. 分离沸点相差较大的互溶液体混合物
C. 容量瓶中转移液体
D. 分离互不相容的两种液体
【答案】B
【解析】
【详解】A项,NaOH溶液能吸收CO2,不吸收CO,长管进气、短管出气可确保CO2被充分吸收,A项能达到目的;
B项,分离沸点相差较大的互溶液体混合物用蒸馏法,蒸馏装置中温度计的水银球应在蒸馏烧瓶支管口附近,B项不能达到目的;
C项,向容量瓶中转移液体时用玻璃棒引流,C项能达到目的;
D项,分离互不相溶的两种液体用分液法,D项能达到目的;
答案选B。
6.下列说法中正确的是( )
A. 液态HCl、固态NaCl均不导电,所以HCl、NaCl均不是电解质
B. NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质
C. 铜、石墨均导电,所以它们是电解质
D. 蔗糖、酒精在水溶液或熔化时均不导电,所以它们是非电解质
【答案】D
【解析】
【详解】A、液态HCl、固体NaCl均不导电,但HCl、NaCl溶于水均电离出阴阳离子而导电,均是电解质,A错误;
B、NH3、CO2的水溶液均导电,但溶液导电是因为二者都与水反应生成电解质一水合氨、碳酸的缘故,不是自身电离产生自由移动的离子,所以NH3、CO2均是非电解质,B错误;
C、铜、石墨均导电,但它们都是单质,所以它们不是电解质,也不是非电解质,C错误;
D、蔗糖、酒精在水溶液或熔融时均不能电离出离子,不导电,所以它们是非电解质,D正确。
答案选D。
7.为除去混在氯化钾中的少量硫酸钾和氯化钙杂质,需进行下列六项操作:
①加水溶解 ②加热蒸发结晶 ③加入过量氯化钡溶液 ④加入过量盐酸 ⑤加入过量碳酸钾溶液 ⑥过滤。正确操作顺序是( )
A. ①③⑤⑥④② B. ①⑤③④⑥②
C. ①③④⑥⑤② D. ①⑤③⑥④②
【答案】A
【解析】
【详解】除去混在氯化钾中的少量硫酸钾和氯化钙杂质,实际上是除去SO42-和Ca2+,先① 加水溶解,再③加入过量氯化钡溶液,除去SO42-,然后⑤加入过量碳酸钾溶液,除去Ca2+和Ba2+,再⑥过滤,最后④ 加入过量盐酸,除去碳酸钾,②加热蒸发结晶即得产品;
答案选A。
8.下列离子方程式书写正确的是( )
A. 铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑
B. AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓
C. 三氯化铁溶液中加入铁粉:
D. FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
【答案】D
【解析】
【分析】本题主要考查离子方程式的书写与判断。
【详解】A.原子数目不守恒应改为:,故A错误;
B.氨水是弱电解质,不能拆成离子形式,应改为:
,故B错误;
C.三氯化铁溶液中加入铁粉的反应为:,故C错误;
D.氯气能把亚铁离子氧化到最高价,即,故D正确;
故答案选D。
9.下列各组物理量中,随取水量的变化而变化的是( )
A. 水的密度 B. 水的沸点
C. 水的物质的量 D. 水的摩尔质量
【答案】C
【解析】
【详解】水的沸点、密度为水的物理性质,与水的量无关,水的摩尔质量为18g/mol,与水的量无关,由可知,水的量越多,物质的量越多,故答案为C。
10.为确定碳酸氢钠固体中是否含有碳酸钠,下列实验操作及判断正确的是( )
A. 观察加热时能否放出气体
B. 观察滴加盐酸时能否放出气体
C. 溶于水中,滴加澄清石灰水,观察是否有沉淀生成
D. 溶于水中,滴加少量氯化钡溶液,观察是否有白色沉淀生成
【答案】D
【解析】
【详解】A.无论是否含有碳酸钠,加热时,碳酸氢钠分解都产生气体,不能确定是否含有碳酸钠,故A错误;
B.碳酸钠和碳酸氢钠加入盐酸都生成二氧化碳气体,不能确定是否含有碳酸钠,故B错误;
C.碳酸钠和碳酸氢钠溶于水中,滴加澄清石灰水,都产生碳酸钙沉淀,不能确定是否含有碳酸钠,故C错误;
D.溶于水中,滴加少量氯化钡溶液,只有碳酸钠产生沉淀,如能观察到白色沉淀生成,说明含有碳酸钠,故D正确;
故答案选D。
11.下列对Na2O2的叙述中,正确的是( )
A. Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物
B. Na2O2能与水反应,所以Na2O2可作干燥剂
C. Na2O2与水反应时,Na2O2只作氧化剂
D. Na2O2与CO2反应时,Na2O2既是氧化剂,又是还原剂
【答案】D
【解析】
【详解】A.Na2O2能与酸反应生成盐和水,还有氧气,所以Na2O2不是碱性氧化物,A项错误;
B.Na2O2能与水反应,生成NaOH和氧气,所以Na2O2不能作干燥剂,B项错误;
C.Na2O2与水反应时,氧元素一部分得电子化合价降低,一部分失电子化合价升高,Na2O2既作氧化剂,又作还原剂,C项错误;
D.Na2O2与CO2反应时,氧元素一部分得电子化合价降低,一部分失电子化合价升高,Na2O2既是氧化剂,又是还原剂,D项正确;
答案选D。
12.在无色透明的溶液中,能够大量共存的离子组是( )
A. Al3+、Ca2+、Cl-、NO3- B. Ba2+、K+、CO32-、Cl-
C. Na+、Cu2+、NO3-、HCO3- D. Na+、Fe2+、Cl-、SO42-
【答案】A
【解析】
【详解】A.Al3+、Ca2+、Cl-、NO3-各离子互不反应,能大量共存,A正确;
B.Ba2+与CO32-反应生成白色沉淀,不能大量共存,B错误;
C.Cu2+呈蓝色,不能在无色溶液中存在,C错误;
D.Fe2+浅绿色,不能在无色溶液中存在,D错误;
答案选A。
13.某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是( )
A. 石蕊 B. AgNO3 C. NaOH D. AlCl3
【答案】D
【解析】
【分析】自来水是由氯气消毒的,氯气溶于水发生反应Cl2+H2OHCl+HClO,所以自来水中含有HCl、HClO和Cl2。
【详解】A.石蕊遇HCl变红,遇HClO褪色,不符;
B.AgNO3遇HCl生成白色沉淀,不符;
C.NaOH与HCl反应生成NaCl,不符;
D.AlCl3不会产生明显药品变质,符合;
答案选D。
14.制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生反应2FeCl3+Cu=2FeCl2+CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,剩余固体不可能是( )
A. 有铜无铁 B. 有铁无铜
C. 铁、铜都有 D. 铁、铜都无
【答案】B
【解析】
【分析】Fe的还原性大于Cu,所以向氯化铁溶液中加入Cu、Fe可能发生的反应有2FeCl3+Cu=2FeCl2+CuCl2、2FeCl3+Fe=3FeCl2、CuCl2+Fe=FeCl2+Cu,且Fe先发生氧化还原反应,据此分析解答。
【详解】A.Fe的还原性大于Cu,所以加入Fe、Cu时Fe先参加反应,当Fe完全反应后,Cu部分反应,则烧杯中有Cu无Fe,故A不选;
B.Fe的还原性大于Cu,所以加入Fe、Cu时Fe先参加反应,如果溶液中有Fe而无铜,则Fe会和铜离子发生置换反应而生成铜,所以不可能出现有Fe而无Cu现象,故B可选;
C.如果铁完全将铁离子还原还剩余,则Cu就不参加反应,所以烧杯中还剩Fe、Cu,故C不选;
D.如果铁离子的量足够大,Fe、Cu完全反应后铁离子还剩余,则烧杯中Cu、Fe都不存在,故D不选;
故选:B。
15.将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,通过一步实验就能加以区别,并只用一种试剂,这种试剂是( )
A. KSCN B. BaCl2 C. NaOH D. HCl
【答案】C
【解析】
【分析】所选择的试剂与氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液结合后出现不同的现象。
【详解】氯化钠溶液中滴加氢氧化钠溶液无明显现象;氯化铝溶液中滴加氢氧化钠溶液,先出现白色沉淀,当氢氧化钠溶液过量后沉淀溶解;氯化亚铁溶液中滴加氢氧化钠溶液,先生成白色沉淀,后白色沉淀逐渐变为灰绿色,最终变为红褐色;氯化铁溶液中滴加氢氧化钠溶液生成红褐色沉淀;氯化镁溶液中滴加氢氧化钠溶液产生白色沉淀;五种溶液中分别加入氢氧化钠溶液,实验现象不同;
答案选C。
16.铁和氧化铁的混合物共2mol,加盐酸后固体全部溶解,共收集到0.5molH2,且溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为( )
A. 0.5mol B. 1.5mol C. 0.75mol D. 1.25mol
【答案】D
【解析】
【详解】根据电子转移守恒,与H+ 反应生成H2 的铁的物质的量等于氢气的物质的量,即:n(Fe)=n(H2 )= 0.5mol,其余的铁则和Fe2 O3 以等物质的量溶于盐酸生成FeCl2,即Fe+ Fe2O3+6H+ =3Fe2+ +3H2 O,参加该反应的铁的物质的量为:n(Fe)=(2mol-0.5mol)=0.75mol,故原混合物中共含铁:0.5mol +0.75mol=1.25mol;
答案选D。
17.根据下列反应判断有关物质还原性由强到弱的顺序是( )
①H2SO3+I2+H2O=2HI+H2SO4
②2FeCl3+2HI=2FeCl2+2HCl+I2
③3FeCl2+4HNO3=2FeCl3+NO↑+2H2O+Fe(NO3)3
A. H2SO3>I->Fe2+>NO B. I->Fe2+>H2SO4>NO
C. Fe2+>I->H2SO3>NO D. NO>Fe2+>H2SO3>I-
【答案】A
【解析】
【详解】①H2SO3+I2+H2O=2HI+H2SO4,I元素的化合价降低,S元素的化合价升高,则H2SO3还原剂,I-为还原产物,还原性:H2SO3>I-;②2FeCl3+2HI=2FeCl2+2HCl+I2中,Fe元素的化合价降低,I元素的化合价升高,则HI为还原剂,Fe2+为还原产物,还原性:I->Fe2+;③3FeCl2+4HNO3=2FeCl3+NO↑+2H2O+Fe(NO3)3中,N元素的化合价降低,Fe元素的化合价升高,则FeCl2还原剂,NO为还原产物,还原性:Fe2+>NO;由此可知,还原性由强到弱的顺序为H2SO3>I->Fe2+>NO,故答案为A。
18.某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子,其中加入足量的Na2O2
固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)( )
A. Na+ B. CO32-、NH4+
C. CH3COO- D. CH3COO-、Na+
【答案】C
【解析】
【详解】向含有大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子的溶液中加入足量的Na2O2,发生的反应依次为:2Na2O2+2H2O =4NaOH+O2↑、NH4++OH-=NH3·H2O、HCO3-+OH-=CO32-+H2O,Na+、CO32-浓度增大,NH4+、HCO3-浓度减小,CH3COO-浓度基本不变,答案选C。
19.下列有关实验操作、现象和解释或结论都正确是( )
选项
实验操作
现象
解释或结论
A
过量的Fe粉中加入HNO3,充分反应后,滴入KSCN溶液
溶液呈红色
稀将Fe氧化为
B
CO2通入BaCl2溶液中
有白色沉淀出现
生成了BaCO3沉淀
C
Al箔插入稀中
无现象
Al箔表面被氧化,形成致密的氧化膜
D
用玻璃棒蘸取浓硝酸点到蓝色石蕊试纸上
试纸先变红色后褪色
浓硝酸有酸性和氧化性
【答案】D
【解析】
【详解】A.过量的Fe粉中加入HNO3,硝酸将铁氧化成Fe3+,接着发生2Fe3++Fe=3Fe2+,充分反应后,滴入KSCN溶液无现象,故A错误;
B.CO2与BaCl2溶液不反应,故B错误;
C.铝在浓硝酸中发生钝化,而在稀硝酸中反应生成硝酸铝、NO和水,故C错误;
D.浓硝酸有酸性,使蓝色石蕊试纸变红,浓硝酸有强氧化性,能使变红的石蕊试纸褪色,故D正确;
故答案选D。
20.现有CuO、FeO、Fe2O3组成的混合物m g,向其中加入100mL 1mol·L-1硫酸,恰好完全溶解,若m g该混合物在过量氢气流中加热充分反应,则冷却后剩余固体的质量为( )
A. (m-0.8)g B. (m-1.2)g
C. (m-1.6)g D. 无法计算
【答案】C
【解析】
分析】金属氧化物与硫酸反应生成硫酸盐和水,由反应CuO~CuSO4,FeO~FeSO4,Fe2O3~Fe2(SO4)3,可知H2SO4的物质的量等于金属氧化物中O元素的物质的量,据此计算金属氧化物中氧元素的质量,金属氧化物的质量减去氧的质量即为金属的质量
【详解】由反应CuO~CuSO4,FeO~FeSO4,Fe2O3~Fe2(SO4)3,可知H2SO4的物质的量等于金属氧化物中O元素的物质的量,n(H2SO4)=0.1L×1mol/L=0.1mol,所以金属氧化物中O的质量为0.1mol×16g/mol=1.6g,若将mg原混合物在足量氢气中加热,使其充分反应,冷却后剩余固体为金属单质,则金属质量为氧化物的质量减去氧的质量,故冷却或剩余金属质量=mg-1.6g=(m-1.6)g,答案选C。
第II卷(非选择题)
21.已知A、B、C、D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①A + B→白色沉淀,加入稀硝酸,沉淀不溶解
②B + D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色
③C + D→白色沉淀,继续加入D溶液,白色沉淀逐渐消失
(1)试推断A________B_________C________D_________(化学式)。
(2)写出下列反应的化学方程式或离子方程式:
①实验②中沉淀由白色转化为红褐色的化学方程式_____________________________,
②C溶液与D溶液反应后生成的白色沉淀溶解于D溶液中的离子方程式_____________。
【答案】(1). BaCl2 (2). FeSO4 (3). AlCl3 (4). NaOH (5). 4Fe(OH)2+O2+2H2O=4Fe(OH)3 (6). Al(OH)3+ OH-=AlO2-+ 2H2O
【解析】
【分析】白色沉淀不溶于稀硝酸应该是硫酸钡,这说明A和B是氯化钡、硫酸亚铁;根据反应②
的现象可知,红褐色沉淀是氢氧化铁,所以B一定是硫酸亚铁,则A是氯化钡,D是氢氧化钠,因此C是氯化铝。
【详解】(1)根据分析可知,A为BaCl2、B为FeSO4、C为AlCl3、D为NaOH;
(2)①氢氧化亚铁与氧气、水反应生成氢氧化铁,化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3;
②氯化铝与氢氧化钠反应生成氢氧化铝沉淀,氢氧化铝溶于氢氧化钠溶于的离子方程式为Al(OH)3 + OH- =AlO2-+ 2H2O。
22.向20 mL AlCl3溶液中滴入2 mol/L NaOH溶液时,得到沉淀的质量与所滴加NaOH溶液的体积有如图关系:
(1)图中A点表示的意义是______________________。
(2)图中B点表示的意义是_____________________。
(3)若溶液中有Al(OH)3沉淀0.39 g,求出用去NaOH溶液的体积________或_______。
【答案】(1). Al3+完全沉淀 (2). Al(OH)3刚好完全溶解 (3). 7.5 mL (4). 17.5 mL
【解析】
【详解】(1)开始AlCl3与NaOH反应Al3++3OH-=Al(OH)3↓,生成Al(OH)3沉淀,NaOH量逐渐增多,Al(OH)3量逐渐增大,到A点时氢氧化钠将AlCl3恰好完全沉淀,Al(OH)3沉淀达到最大量,故答案为:Al3+完全沉淀;
(2)Al(OH)3沉淀达到最大量后,再加NaOH,发生Al(OH)3+OH-=AlO2-+2H2O,沉淀量又逐渐减少,到B点时Al(OH)3与NaOH恰好完全反应生成NaAlO2,沉淀完全溶解消失,故答案为:Al(OH)3刚好完全溶解;
(3)0.39 g Al(OH)3的物质的量==0.005mol,当NaOH溶液不足时,生成0.39 g Al(OH)3所需NaOH的物质的量为:0.005mol×3=0.015 mol,需要NaOH溶液的体积==0.0075L=7.5mL;当NaOH溶液过量时,还剩余0.39 g Al(OH)3,剩余0.39 g Al(OH)3
溶解可以消耗0.005molNaOH,故共消耗NaOH的物质的量=0.02L×2mol/L-0.005mol=0.035 mol,需要NaOH溶液的体积==0.0175L=17.5mL。
23.学生利用下图所列装置进行“铁与水蒸气反应”的实验。(图中夹持及尾气处理装置均已略去)
(1)回答下列问题:所用铁粉中若有杂质铝,欲除去不纯铁粉中混有的铝粉可以选用的试剂为____________(填序号)。
A.稀盐酸 B.氢氧化钠溶液 C.浓硫酸 D. FeCl3溶液
此步涉及反应的离子方程式为________________________。经除杂后的铁粉进一步干燥后装入反应容器。
(2)反应发生后装置B中发生反应的化学方程式是______________________。
【答案】(1). B (2). (3).
【解析】
【分析】A装置提供水蒸气,B中水蒸气与铁发生反应生成四氧化三铁和氢气,C为氢气收集装置,D为干燥装置,E中氢气与氧化铜反应生成铜和水(验证产生了氢气)。
【详解】(1)除铁粉中的杂质铝,应该选一个只和铝反应而不和铁反应的试剂,
A.稀盐酸和铁、铝均反应,A错误;
B.氢氧化钠溶液只和铝反应,不和铁反应,B正确;
C.铁、铝在浓硫酸中钝化,C错误;
D.氯化铁溶液和铁、铝都反应,D错误;
涉及的反应为铝和氢氧化钠反应生成四羟基合铝酸钠和氢气,方程式为: ;
故答案为:B;;
(2)铁和水蒸气高温下生成四氧化三铁和氢气,方程式为:,
故答案为:。
24.实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是__________。
(2)在容量瓶的使用方法中,下列操作不正确的是____________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)根据计算用托盘天平称取的质量为______g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度_____0.1mol/L(填“大于”“小于”或“等于”)。
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为_______mL,如果实验室有15mL、20mL、50mL量筒,应选用______mL量筒最好。
【答案】(1). A、C (2). 烧杯、玻璃棒、500mL容量瓶 (3). BCD (4). 2.0 (5). 小于 (6). 13.6 (7). 15
【解析】
【详解】(1)配制一定物质的量浓度溶液的一般步骤:计算、称量或者量取、溶解或者稀释、移液、洗涤、定容、摇匀,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以用不到的仪器:平底烧瓶、分液漏斗;还缺少的仪器:烧杯、玻璃棒、500mL容量瓶;
(2)A.容量瓶是带有活塞的仪器,使用前要检查是否漏水,故A正确;
B.容量瓶用蒸馏水洗净后,不能够使用待配溶液润洗,否则导致配制的溶液浓度偏高,故B错误;
C.容量瓶是精密定量仪器,只能用于配制一定物质的量浓度的溶液,不能用于溶解,应该在烧杯中溶解固体,故C错误;
D.容量瓶是精密定量仪器,只能用于配制一定物质的量浓度的溶液,不能用于稀释浓溶液,应该在烧杯中稀释浓溶液,故D错误;
E.摇匀的正确操作为:盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次,故E正确;
答案为BCD;
(3)需要0.1mol/LNaOH溶液450mL,应选择500mL容量瓶,实际配制500mL溶液,需要溶质的质量=0.1mol/L×0.5L×40g/mol=2.0g;若定容时仰视刻度线,导致溶液体积偏小,所配溶液浓度偏低;
(4)浓H2SO4的物质的量浓度c=mol/L=18.4mol/L,稀释前后溶质的物质的量不变,设需要浓硫酸的体积为V,则:V×18.4mol/L=0.5L×0.5mol/L,解得V=13.6ml,应选用15mL规格的量筒。